弱酸・弱塩基遊離反応
概要
「弱酸・弱塩基遊離反応」とは、弱酸由来の塩・弱塩基由来の塩から弱酸・弱塩基が発生する反応のこと。弱酸由来の塩に強酸を加えると弱酸が、弱塩基由来の塩に強塩基を加えると弱塩基が遊離します。強いやつが弱いやつを追い出す反応というイメージですね。
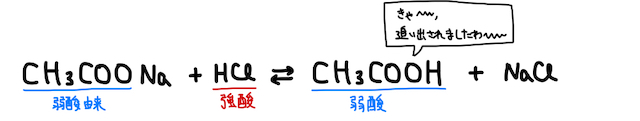
この反応はそもそも、弱酸(弱塩基)は電離して
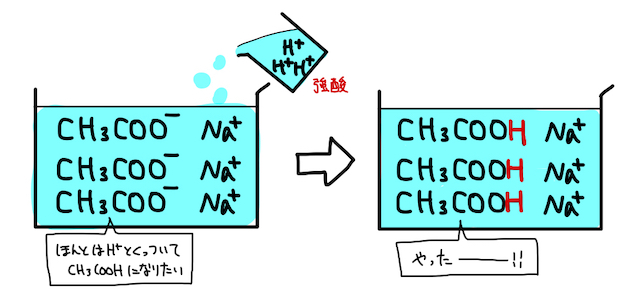
詳細
弱酸由来の塩・弱塩基由来の塩
化学式を見れば、その塩(イオン結晶)がどんな中和反応から生じるものかを判別できます。
まず原則、金属+非金属からなる物質は、金属陽イオンと非金属陰イオンのイオン結晶(塩) です。つまり、化学式を見ればイオン結晶であることはわかります。
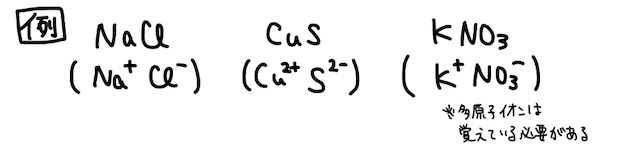
続いて、そのイオン結晶が中和反応で生じるとすると、結論金属陽イオンから
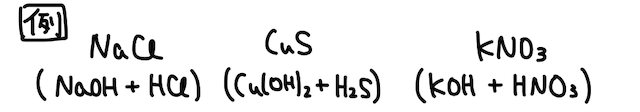
以上により、ある塩がどんな酸・塩基由来であるかを考えられます。あとは酸と塩基の強弱を覚えていれば、弱酸由来や弱塩基由来を判別可能です。
仕組み
弱酸由来の塩である
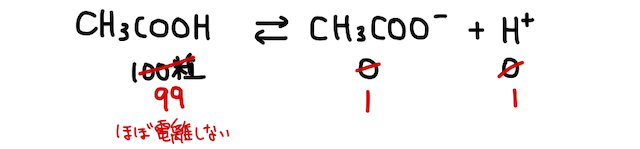
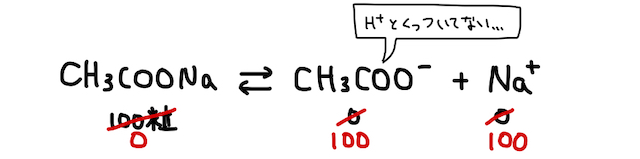
そんなところに、大量に
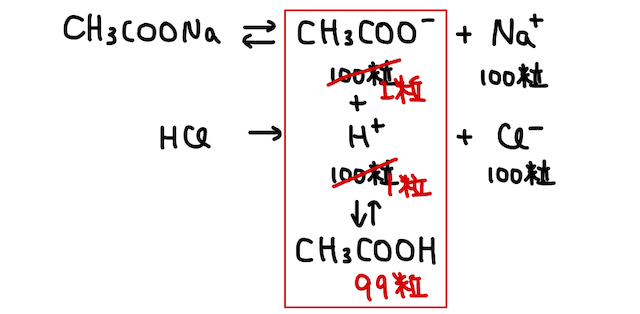
つまり、最初に「強いものが勝つ」的なことを言いましたが、実際の仕組み的には弱酸側のわがままで反応が起こっている雰囲気ですね。
反応式の書き方
塩に含まれる弱酸(弱塩基)イオンの価数分、
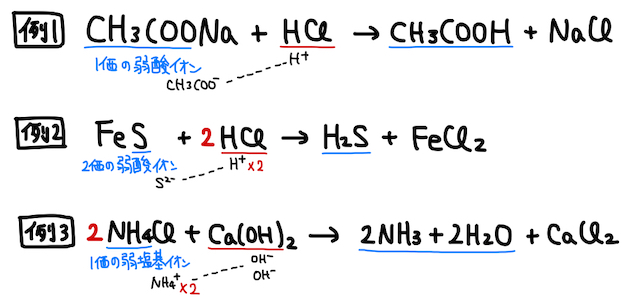
少しだけ発展
弱酸・弱塩基遊離反応は、相対的に酸(塩基)の強さに差があれば、弱酸同士(弱塩基同士)でも起こります。
たとえば、同じ弱酸である酢酸
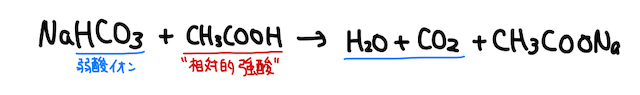
これらは、有機化合物の分離などで頻出です。
補足
- (*補足1)ここで実際には、塩の加水分解が起こります。ただし弱酸遊離の影響の方が大きいので、強酸を加えてしまえば関係ありません。
関連動画






