溶媒抽出
概要
「溶媒抽出」とは、混ざり合わない溶媒への溶解性の違いによって混合物を分離する方法のこと。たとえば、アニリンは有機溶媒に溶けやすいですが、中和して官能基がイオンになっている場合は水に溶けやすくなり、有機物から分離することができます。
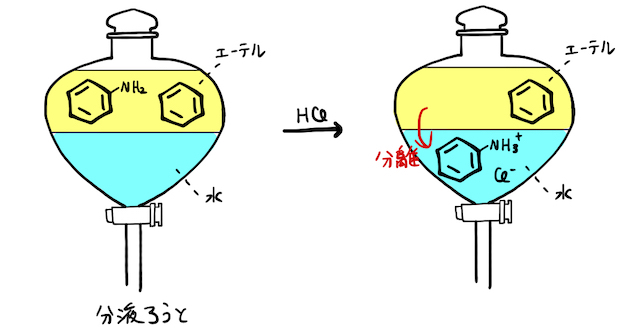
有機化合物では主に、「分液漏斗」を用いて分離を行います。
詳細
溶媒への溶解性
極性溶媒と無極性溶媒は混ざり合いにくいため、水と油のように混ぜても2層に分離します(*補足1)。ここに極性物質を加えれば極性溶媒側に、無極性物質を加えれば無極性溶媒側に溶けます。
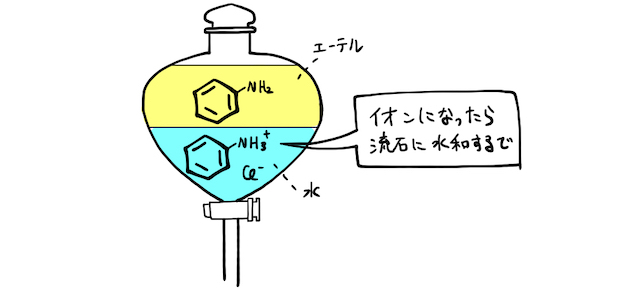
たとえば芳香族化合物では、無極性のベンゼン環が大部分を占めるため、原則無極性溶媒に溶けます。しかし、官能基にイオンを持つ場合(つまり塩になっている場合)は、極性溶媒に溶けるようになります。
溶媒抽出の手順
溶媒抽出は、溶媒への溶解性の違いを利用した分離操作です。ここでは芳香族化合物の分離に絞って、以下の具体例を用いて手順を説明します。
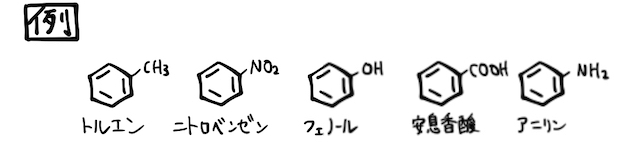
アニリンのみが塩基性なので、塩酸
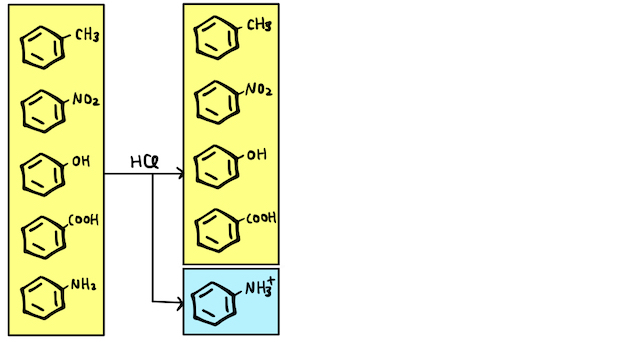
有機層のみを取り出して分離を続けます。同じ発想で考えたいですが、安息香酸とフェノールが共に酸性なので、たとえば水酸化ナトリウム
酸の強さはカルボン酸>炭酸>フェノールなので、炭酸の塩である炭酸水素ナトリウムを加えることでカルボン酸のみを反応させることができます。
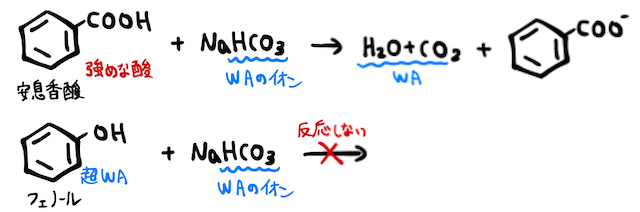
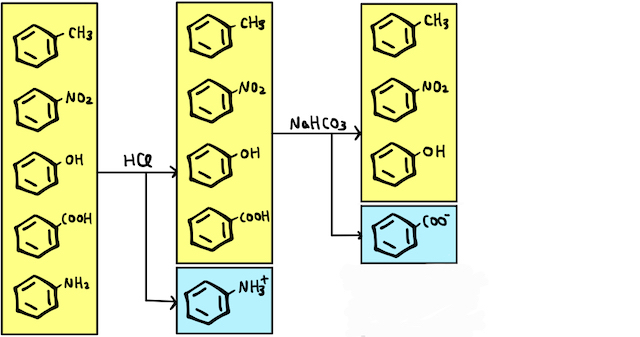
これによって、カルボン酸のみが塩となり、水に溶けることで分離されます。
再び有機層のみを取り出して分離を続けます。以上でフェノールのみが酸性物質となったので、水酸化ナトリウムを加えて中和することで、塩になったフェノールを水に溶かして分離できます。
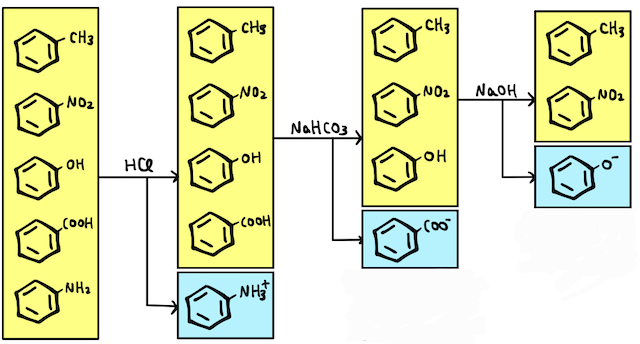
最後に残ったニトロベンゼンとトルエンは、共に中性なので化学反応による分離が難しいです。そこで、沸点の違いを利用した「分留」によって分離します。
補足
- (*補足1)雑い表現でいえば、極性分子は磁石、無極性分子はただのボールのイメージです。磁石同士は引っ張り合うのでまとまりますが、ボールは特に何も起こらないので、結果的に磁石の塊とボールの塊に分かれることになります。 そして、溶媒の密度が小さい方が上層に、大きい方が下層になります。たとえばジエチルエーテルは水より軽いため、上層がエーテル、下層が水となります。一方、四塩化炭素やクロロホルムなどは水より思いため、上層が水、下層が有機物となります。
関連動画
関連用語






