気体分子運動論
はじめに
気体の圧力や体積といった、気体分子がめちゃくちゃたくさん集まったものについての情報を、1個1個の気体分子についての質量や速度といった情報で表せないか考えてみよう。
気体全体の圧力や体積(
を示すのがゴール。
結構長い話になるけども、今から紹介していくストーリーは教科書にも載っていて、よく 「気体分子運動論」 と呼ばれ、このまままるっと入試に出ることも多いので、自力で最初から最後まで再現できるように身につけておこう。
状況の設定
一辺の長さが
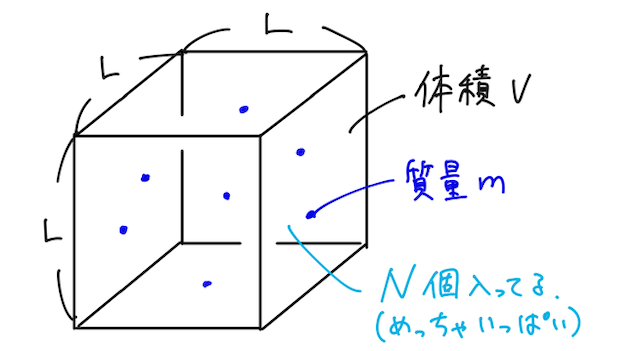
現実の気体をいきなり考えられるほど世の中甘くないので、議論できるように理想的な設定を仮定していく。
仮定①:分子は立方体の容器内をビュンビュン飛び回り、立方体の壁に衝突しまくるが、その衝突は 弾性衝突 であるとする。
仮定②: 分子の数(
仮定③: 分子間にはたらく力を無視できる理想気体としての単原子分子を考える。このとき、気体の内部エネルギーは、それぞれの気体分子の運動エネルギーの合計と考えてよい。
これらを認めた上で、導出を見ていこう!
内部エネルギーの式の導出
まず、気体全体の圧力や体積(
1個1個の分子の衝突について、じっくり考えてみる。
立方体の辺に沿って例えば左下のように
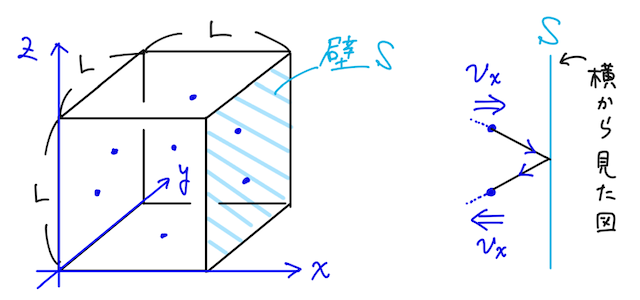
まずは
このとき、仮定①より衝突後の速度は
となる。作用反作用の法則から、1個の分子の衝突により、気体分子から壁が受ける力積の大きさは、
と求められる。
また、一度壁に衝突した気体分子が、向かいの壁でも衝突し、再び同じ壁
と求められるので、まとめると、壁
よって、時間
となる。
この間に、壁
と求められる。
これはあくまでも1個の気体分子から受ける平均の力の大きさであり、壁
と表される。
ここで、他の軸の方向の速度も考えてみると、まず分子の速度
であるから(下の図で、三平方の定理で考えてみよう)
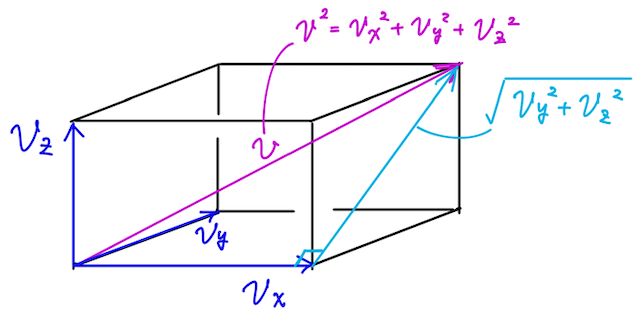
が成り立ち、さらに今回は仮定②の分子運動の等方性より
としてよいので、
が成り立つ。
よって、これを
と整理できる。
ここまでくれば、平均の力の大きさ
となるので、
が成り立つ。
つまりこれで、気体全体の圧力や体積(
ここで、気体の温度を
なので、
を得る。左辺が気体分子1個の運動エネルギーの形になるように変形すると
となる。ここでアボガドロ定数を
なので、
と表せる。ここで、
が導かれる。
この、気体定数をアボガドロ定数で割った定数
となる。
さらに、単原子分子理想気体の内部エネルギーは、仮定③により、気体分子の運動エネルギーの総和で求められるので、
となり、確かに単原子分子の内部エネルギーの式が示された。
補足
余裕がある人は、気体の二乗平均速度という物理量についても求め方を学んでおこう。
関連動画