概要
「フェーリング反応」とはずばり、の赤色沈澱を生じさせることで、還元性を持つアルデヒドを検出する反応のこと。を含むフェーリング液という試薬にアルデヒドを加えて加熱すると、アルデヒドによってが還元され赤色沈澱が生じます。
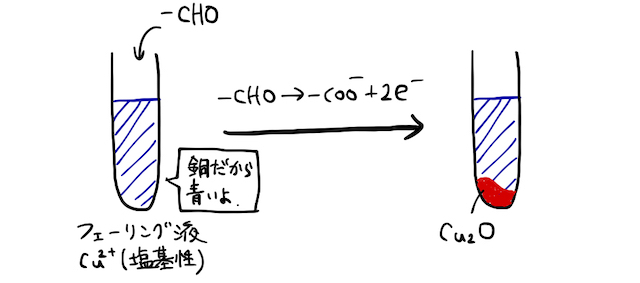
銀鏡反応と同様の仕組みで、還元性を持つホルミル基に対して、イオン化傾向の小さい銅イオンが酸化剤として働いています。
以上は塩基性条件で行いますが、はに対して沈澱を作ってしまいます。そこでフェーリング液には、硫化銅と水酸化ナトリウムに加えて、を錯イオンにして保護するために酒石酸ナトリウムが加えられています。
詳細
反応の仕組み
ホルミル基は、塩基性条件下で酸化されやすい(=還元剤になりやすい)です。カルボニル基では、電気陰性度の大きい酸素が電子対を引っ張って、炭素が少しプラスになります。塩基性下ではそこにがぶつかります。
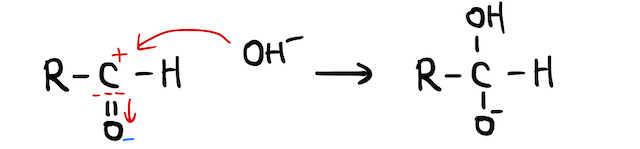
ここに酸化剤がやってきて、の結合から電子を奪い取ることでカルボン酸になります。
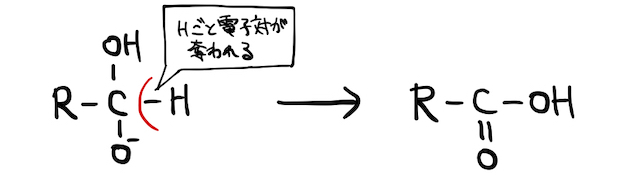
以上の性質を利用し、塩基性下でイオン化傾向が小さい銅イオンを酸化剤として働かせるのがフェーリング反応です。
ただし、は塩基性で不溶性の塩を生じてしまいます。そこでフェーリング液では、酒石酸ナトリウムを加えて錯イオンを作ることで、を保護しています(*補足1)。
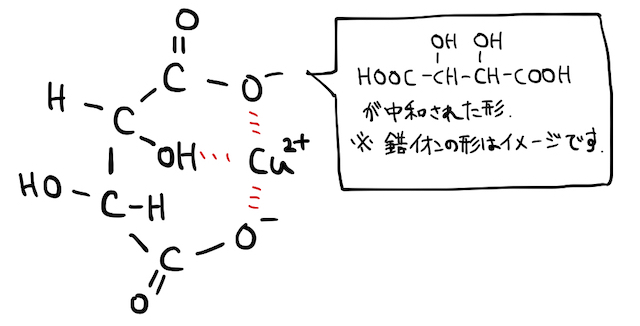
以上を踏まえて、フェーリング反応の半反応式は以下のようになります。アルデヒドでは還元力が足りず、銅までは還元できずにで止まっているイメージです。また塩基性条件なので、発生するカルボン酸は塩になっていることに注意です。
例外
ホルミル基を持つ物質のうち、ギ酸とベンズアルデヒドはフェーリング反応を起こしづらいです。大学入試であえてこんな細かい知識を聞くことは少ないですが、性格の悪い大学はドヤ顔で出題してくる可能性があります。
ギ酸はカルボキシ基を持つため、酒石酸イオンと同様にと錯イオンを作るため反応が起こりづらいです。ベンズアルデヒドの方はもっと複雑ですが、ざっくりいえばベンゼン環とカルボニル基の相性がよく、安定性が高いので反応が起こりづらいです。
補足
- (*補足1)このように、1つの配位子で2ヶ所以上配位している錯体を「キレート錯体」といいます。名前を覚えている必要はありませんが、友達とフェーリング反応で盛り上がったときに「あー、キレート錯体のね」とわかりきった感じで言うとカッコいいです。でもちょっと鬱陶しくもあります。
また、
- 例外ではあえて「起こりづらい」と書いておきました。化学反応は実際のところ反応条件によるので、濃度や温度次第では反応が起こることもあります。
また過去のセンター試験で、ギ酸の還元性の確認において、フェーリング反応を利用する問題があります。しかし指摘を受けてか、その後はすべて銀鏡反応を利用する問題文になっています。まあ早い話、この辺りの知識は複雑なので、疑義が出ないように大抵銀鏡反応で出題されると思うので、例外の知識はほどほどに覚えておけば十分だと思います。









