アルコール
概要
「アルコール」とは、ヒドロキシ基
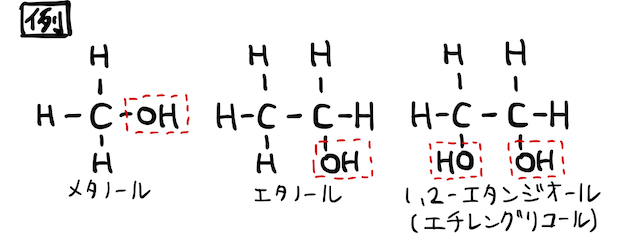
アルコールは比較的反応性が高く、
- (1) 金属
との反応 - (2) アルコールの酸化
- (3) 脱水反応
- (4) エステル化
など、さまざまな反応を起こします。特に(2)はアルコールの種類ごとに生成物が異なって覚えるのが大変です。でも超頻出だから頑張って覚えよう( ͡° ͜ʖ ͡°)
詳細
アルコールとは
ヒドロキシ基
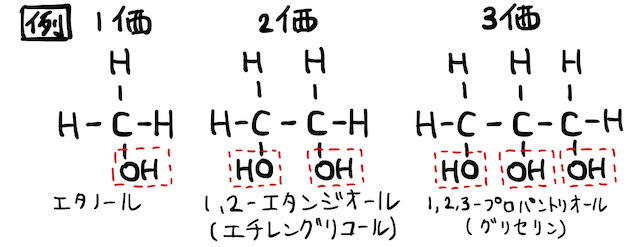
また、
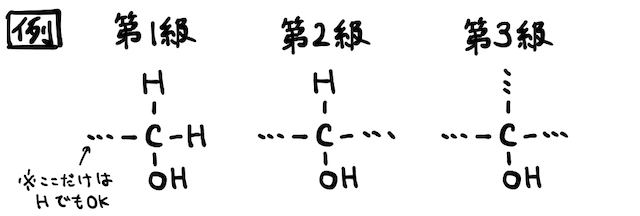
なんでこんな分類するのかちょっと不思議ですが、実はこれにより酸化のされ方などの反応性が変わってきます。続いて説明する「(2)酸化反応」と合わせて理解しておきましょう。
アルコールの反応
アルコールは、電気陰性度が大きい酸素
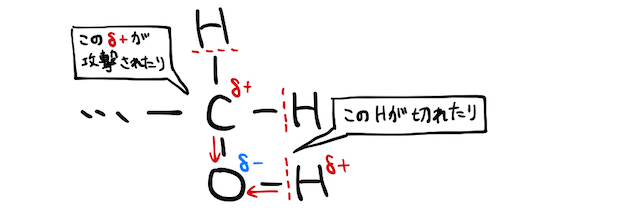
これによって、水素
(1) 金属
電荷の偏りにより、アルコールはほんの少し
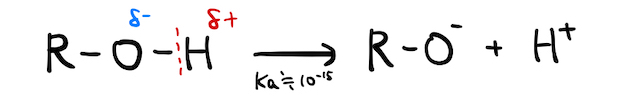
しかし、そこに還元性激強金属の
ちょうど無機化学のときに勉強した、金属
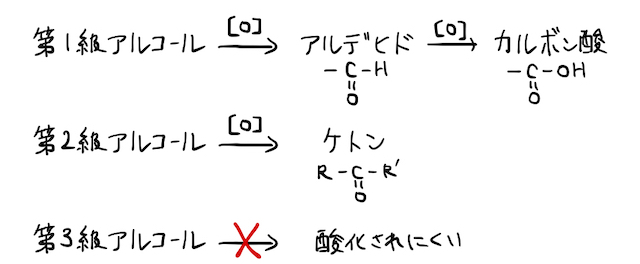
(2) 酸化反応
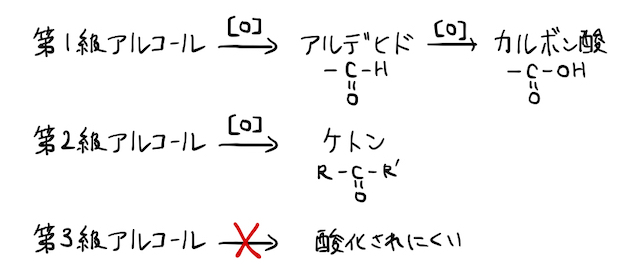
ヒドロキシ基の電荷の偏り目掛けて酸化剤が攻撃し、電子が奪われる酸化反応が起こります。ただし、第何級アルコールなのかによって反応の結果が変わります。最低限、
- 第1級アルコールは、アルデヒドを経てカルボン酸になる
- 第2級アルコールは、ケトンになる
- 第3級アルコールは、酸化されづらい
と言う結果は覚えておきましょう。
気になる人向けに、超雑に仕組みを説明してみます。ヒドロキシ基中の酸素によって電子対が引っ張られ、比較的電気陰性度が小さい水素が剥がされてしまいます。その結果残された電子対で
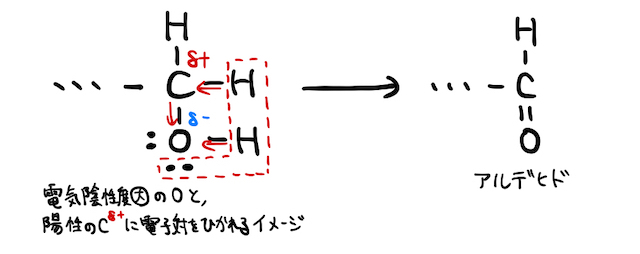
以上は偉い人に怒られそうな雑説明ですが、反応の暗記の手助けになりそうならふわっと参考にしてみてください。もっと硬派なガチ説明を御所望なあなたは「アルコールの酸化」の辞書をチェックしてみてください。
(3) 脱水反応
脱水剤の濃硫酸を加えて100℃以上まで加熱することで、
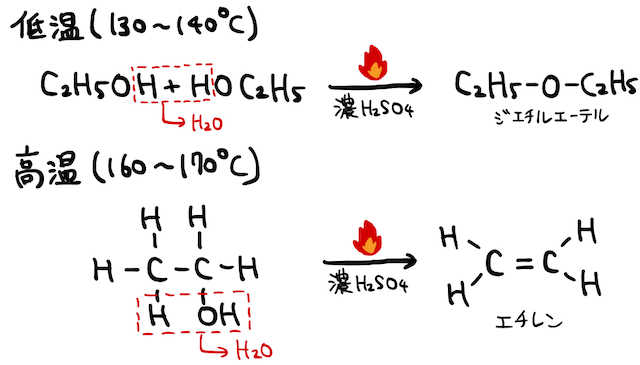
これらを区別しないと解けない問題も出るので、細かいですが頭に入れておきましょう。
(4) エステル化
アルコールは、カルボン酸と脱水縮合することでエステルになります。エステル化は、構造決定問題でも超頻出の反応です。
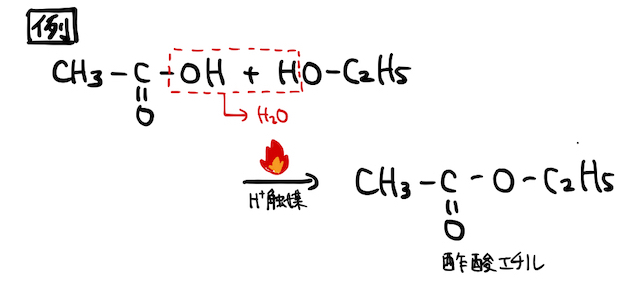
カルボン酸中のカルボニル基
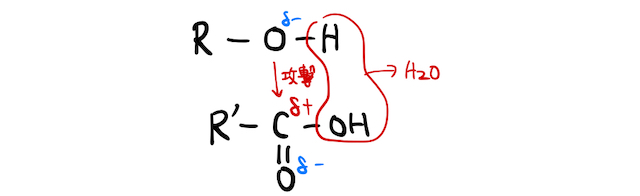
補足
- (*補足1)全然論理的な話じゃないですが、今人的には「高温だと分子のスピードが速く、2分子が隣り合って脱水している暇がない」と覚えています。感覚が合う人は参考にしてみてね。
関連動画
関連用語





