水のイオン積
概要
「水のイオン積
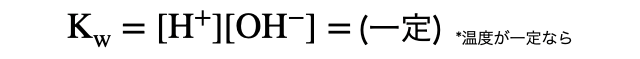
詳細
化学基礎向けの説明
実は水の電離は少し複雑なことが起こっています。でも化学基礎で求められるのは
水のイオン積は、水素イオン濃度
かけ算して一定の値ということは、

これを利用すれば、
一般的な説明
水は以下のような化学平衡の状態にあります。
このときの平衡定数は、
ただし水溶液中では普通水が大量にあるので
平衡定数
補足
- シーソーゲームは、抜きつ抜かれつの大接戦のことです。
- (*注1)例えば1L=1000gの水には1000/18≒56molほどの水分子があるので、水が電離していないとすれば
です。そんな中、純水なら くらいなんだから、電離した水も くらい。よって電離後の水の濃度はだいたい となります。このように水が大量にあるから電離によって減る分は無視できるということです。
関連動画
関連用語





