ルシャトリエの原理
概要
「ルシャトリエの原理」とは、化学平衡に変化を与えるとその変化を打ち消す方向に平衡が移動すると言う原理のこと。ルシャトリエさんの綴りはLe Chatelierだから「ル・シャトリエ」と読むのが正確ですが、実際わざわざそう読んでいると鼻につきます。清少納言を「清・少納言」と読むのも同様です。
化学平衡状態に対して、濃度・圧力・温度に変化を与えると一時的に平衡が崩れて非平衡状態になることがあります。しかし、十分な時間が立てば化学反応がどちらかに進み再び新たな平衡状態に落ち着きます。このとき、濃度・圧力・温度の変化を打ち消す方向に反応が進む、というのがルシャトリエの原理です。 とてもざっくり言えば「出る杭は打たれる」的なことです。
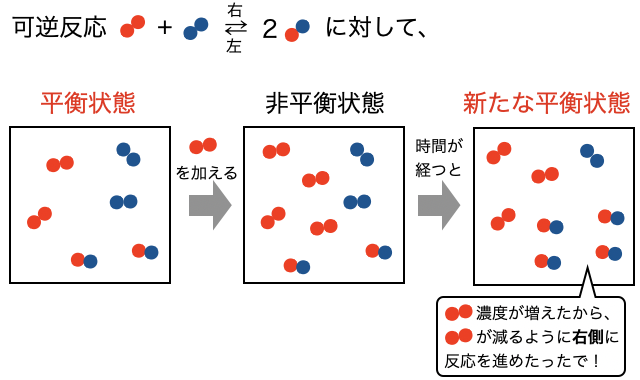
ルシャトリエの原理は、濃度・圧力・温度の変化で成り立つものです(*注)。物質量や体積などを変化させた場合、以上3つの変数に置き換えて考える必要があります。
例
簡単な例

(1)温度・体積一定で、
体積一定で
(2)圧力一定で、温度を上げる。
「反応系の温度が上がる」という変化が起これば、ルシャトリエの原理より反応系の温度が下がる方向へ反応が進むはずです。この反応は発熱反応なので、反応が右に進めば放熱されて空間が温まり、左に進めば吸熱されて空間が冷えます。ということで、温度が下がる=吸熱方向の左向きに反応が進みます。
(3)温度一定で、全圧を上げる。
「反応系の全圧が上がる」という変化が起これば、ルシャトリエの原理より反応系の全圧が下がる方向へ反応が進むはずです。この反応は「4粒の分子が2粒のアンモニア分子になる」と言う反応なので、反応が右に進んだ方が粒子数が4→2と少なくなります。よって、粒子数が下がり全圧が下がる右向きに反応が進みます。
ちょいムズな例

まず前提として平衡定数のときに確認した通り、固体は平衡の移動に影響しません。つまり、平衡を考えるにあたっては
(1)温度一定で、体積を小さくする。
ルシャトリエの原理を適用できるのは、濃度・圧力・温度の変化に対してです。よって体積の変化はこれらに読み替えて考える必要があります。たとえば、体積を小さくすれば全圧が大きくなるので、ルシャトリエの原理より全圧が小さくなる方に反応が進むはずです。
(2)温度・圧力一定で、触媒を加える。
平衡定数で確認した通り、触媒は反応速度を変化させるだけで平衡状態には関係ありません。よって触媒を加えても平衡状態は維持されたままで、平衡が移動することはありません。
(3)温度・体積を一定に保ったまま、アルゴンを加える。
出ました、(3)(4)は受験生全員(筆者調べ)が悩む問題です。これを理解するには、分圧などの気体の基礎知識を理解している必要があります。不安があれば確認しておきましょう。
まず結論から言うと、温度・体積一定の容器にアルゴンが入ってきても、
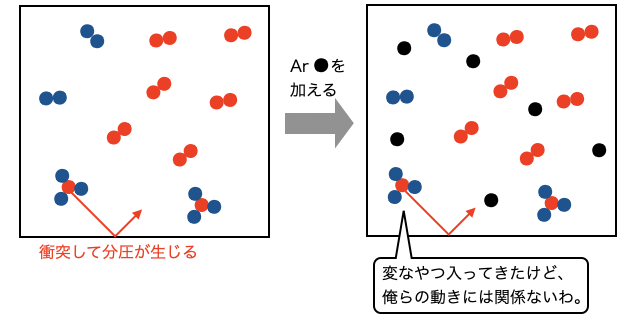
よって、反応系としては何も変化が起こっていないため、平衡が移動することはありません。もちろん、貴ガスのアルゴンが化学反応を起こすこともありません。
(4)温度・圧力を一定に保ったまま、アルゴンを加える。
次は圧力(全圧)を一定に保った場合です。もし体積一定のままアルゴンを加えれば(3)の通り全圧が増えてしまうので、全圧一定に保つには体積を大きくする必要があります。
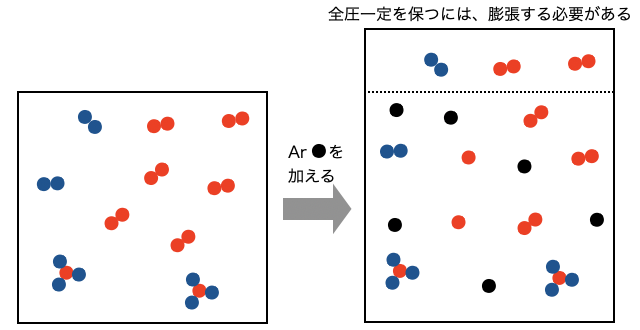
先ほど(3)で見た通り、ただアルゴンが入るだけなら反応系的には何も変化しないはずなのに、体積が大きくなってしまっています。つまり反応系の圧力は小さくなってしまうので、ルシャトリエの原理より粒子数が大きくなって圧力が大きくなる右向きに反応が進みます。
補足
- (*注)2つの塩水を混ぜても濃度が変わらない・窓を開けて部屋の中と外の空気を混ぜても圧力が変わらない・同じ温度の水を混ぜても温度が変わらない、という性質を持つ変数を「示強変数」などと呼びます。ルシャトリエの原理が成り立つのはこれら示強変数に対してです。一方、物質量や体積は2つ足し算すればそれだけ大きくなる「示量変数」です。
この用語を含むファイル
関連動画
関連用語





