配位結合
概要
「配位結合」とは、片方の原子だけが電子対を差し出して作られる結合のこと。不対電子を1個ずつ出し合う共有結合に対して、配位結合では片方が2個(非共有電子対)・もう片方が0個出し合って結合します。
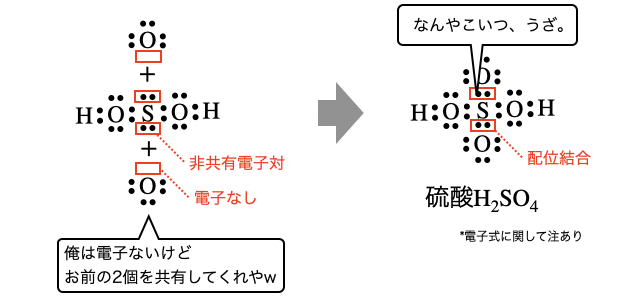
ただし結合によっては共有結合と配位結合を区別できないこともあります。
詳細
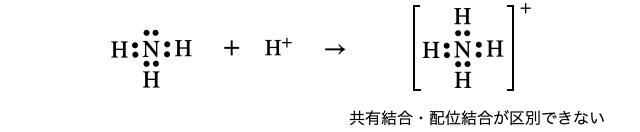
たとえば、アンモニア

このときできるアンモニウムイオン
またオキソ酸や酸化物などでも、酸素
補足
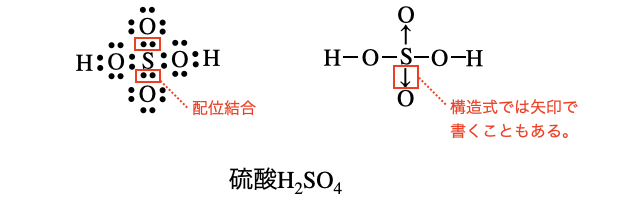
- 配位結合を区別して表記する場合、構造式の価標を「→」で書きます。
- Nagira Academyさんの動画・映像授業Try ITさんの動画などでもわかりやすく解説をされています!
- 正確な硫酸の電子式は以下です。ただしとりあえず「片方が非共有電子対にくっつく」というイメージがまずは大事なので、細かい部分は目をつむっても大丈夫!

この用語を含むファイル
関連動画







